|
■ 制品内容 (Code No.: RR019A : 100 次量*1)
|
AMV Reverse Transcriptase XL (5 U/μl) (Avian Myeloblastosis Virus来源)
|
50 μl
|
|
RNase Inhibitor (40 U/μl)
|
25 μl
|
|
Random 9 mers*2 (50 pmol/μl)
|
50 μl
|
|
Oligo dT-Adaptor Primer (2.5 pmol/μl)
|
50 μl
|
|
RNase Free dH2O
|
1 ml
|
|
TaKaRa Ex Taq HS (5 U/μl)
|
25 μl
|
|
M13 Primer M4*2 (20 pmol/μl)
|
50 μl
|
|
10 × RT Buffer [100 mM Tris-HCl (pH8.3),500 mM KCl]
|
1 ml
|
|
5 × PCR Buffer
|
1 ml
|
|
dNTP Mixture (各10 mM)
|
150 μl
|
|
MgCl2 (25 mM)
|
1 ml
|
|
Control R-1 Primer*2 (20 pmol/μl) (Positive Control RNA下游引物)
|
25 μl
|
|
Control F-1 Primer*2 (20 pmol/μl) (Positive Control RNA上游引物)
|
25 μl
|
Positive Control RNA*3 (2 × 105 copies/μl)
(Transcribed poly(A)+ RNA of pSPTet3 plasmid)
|
25 μl
|
|
|
|
*1:1次反应即10 μl RT及 50 μl PCR
|
|
*2:引物序列
|
|
引物名称
|
各引物序列
|
|
Random 9 mers
|
5′-(P)NNNNNNNNN-3′
|
|
Oligo dT-Adaptor Primer
|
包含dT区域及M13 Primer M4序列。
|
|
Control F-1 Primer
|
5′-CTGCTCGCTTCGCTACTTGGA-3′
|
|
Control R-1 Primer
|
5′-CGGCACCTGTCCTACGAGTTG-3′
|
|
M13 Primer M4
|
5′-GTTTTCCCAGTCACGAC-3′
|
|
|
*3:Positive Control RNA
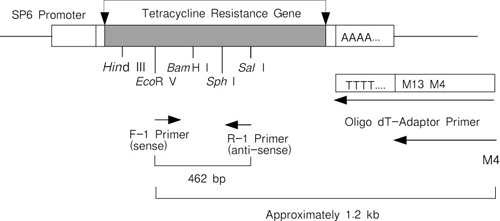
本试剂盒中的Control RNA是以pSPTet3质粒 (质粒中的SP6启动子下游插入长约1.4 kb的pBR322来源的DNA片段,其DNA片段上含有抗四环素基因) 为模板由SP6 RNA聚合酶经体外转录而得到的。Control RNA (约1.4 kb) 是带有30个A碱基的具有Poly(A)+ 尾的RNA。当把Control RNA经RT-PCR合成的双链cDNA插入质粒时,该质粒便可获得四环素抗性。Control RNA简图见图1。
|
|
图1. Positive Control RNA:使用各种引物所能扩增的DNA片段
|
■ 制品说明
PCR (Polymerase Chain Reaction;聚合酶链式反应) 是一种体外扩增DNA的简单而有效的方法。虽然原理上PCR法是扩增DNA,RNA不能直接被扩增,但是经过反转录酶的作用把RNA反转录成cDNA后,PCR法便可应用于RNA的解析了。目前,此方法已广泛应用于RNA的构造解析、cDNA的克隆及RNA水平上的表达解析等多种领域。
TaKaRa RNA PCR Kit Ver.3.0是使用AMV (Avian Myeloblastosis Virus) 由来的反转录酶将RNA合成cDNA,然后在同一反应管中使用Hot Start PCR用TaKaRa Ex Taq HS DNA聚合酶扩增此cDNA的RT-PCR试剂盒。本试剂盒含有从RNA到cDNA,然后使用PCR法扩增此cDNA所需的全部试剂,可实现简单高效的RNA分析。
本试剂盒中的Oligo dT-Adaptor Primer的特殊设计,大大地提高了Poly(A)+ RNA 3′端区域的cDNA合成效率。Hot Start PCR用DNA聚合酶TaKaRa Ex Taq HS的应用,避免扩增前由于错配或引物二聚体产生的非特异性扩增。
■ 保存
-20℃。
■ RNA LA PCR的原理
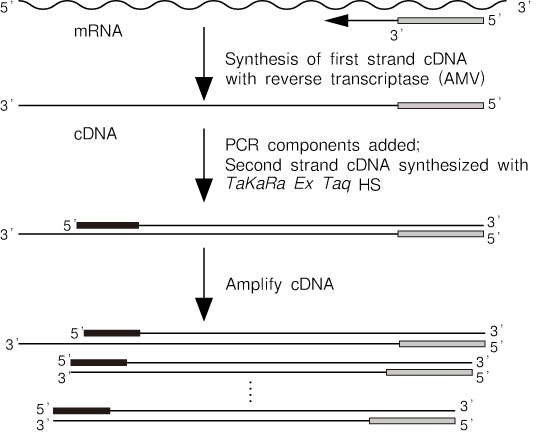
本试剂盒使用AMV由来的反转录酶由RNA合成cDNA,并可在同一反应管中使用TaKaRa Ex Taq HS扩增此cDNA。Random 9 mers、Oligo dT-Adaptor Primer或特异性下游引物等均可作为反转录引物用于cDNA合成。Oligo dT-Adaptor Primer同时适用于3′-RACE实验。
|
|
图2. RNA PCR的原理
|
|
|
|
■ 特点
|
|
RNA模板
|
适用于所有RNA
|
|
扩增片段大小
|
≤5 kb
|
|
反转录酶
|
AMV Reverse Transcriptase XL
|
|
DNA Polymerase
|
TaKaRa Ex Taq HS
|
|
RNase Inhibitor
|
必须使用 (Kit中含有)
|
|
合成第一条cDNA链的引物
|
Random 9 mers、Oligo dT-Adaptor Primer或 特异性下游PCR Primer 可供选择
|
|
3′-RACE法
|
RT反应时使用Oligo dT-Adaptor Primer,PCR反应时下游引物使用M13 Primer M4
|
|
操 作
|
在同一反应管中进行 (反转录酶在进行PCR反应前须进行高温失活)
|
|
|
|
|
|
■ 反转录反应时Primer的选择
|
|
Random 9 mers
|
适用于长的或具有Hairpin构造的RNA。包括rRNA、mRNA、tRNA等在内的所有RNA的反转录反应都可使用本引物。 用Random 9 mers合成的cDNA进行PCR反应时,必须使用特异性引物。
|
|
Oligo dT-Adaptor Primer
|
适用于具有Poly(A)+ Tail的RNA。(注意:原核生物的RNA、真核生物 Primer 的rRNA及tRNA以及某些种类的真核生物的mRNA不具有Poly (A)+ Tail)。 本Primer设计巧妙,反转录效率高。反转录反应后,可用M13 Primer M4进行3′-RACE实验。
|
|
特异性下游PCR Primer
(PCR时的下游引物)
|
因其必须与模板序列互补,所以只适用于Target序列已知的情况。
|
|
|
■ 注意事项
1. 当同时需要进行数次反转录反应或PCR反应时,应先配制各种试剂的混合液 (Master Mix;其中包括RNase Free dH2O、Buffer、dNTP Mixture、MgCl2等),然后再分装到每个反应管中。这样,可使所取的试剂体积更准确,减少试剂损失,避免重复分取同一试剂。同时也可以减少实验操作或实验之间产生的误差。
2. 使用Reverse Transcriptase、RNase Inhibitor、TaKaRa LA Taq 酶等酶类时,应轻轻混匀,避免起泡;分取之前要小心地离心收集到反应管底部;由于酶保存液粘度高,分取时应慢慢吸取。
3. 酶制品应在实验前才从-20℃中取出,使用后也应立即放回-20℃中保存。
4. 分装试剂时务必使用新的枪头 (Tip),以防止样品间污染。
5. 最佳的PCR条件,因PCR扩增仪的不同而不同,所以在使用您的样品之前最好先试做一下Control反应,以确定最佳的PCR条件。